

ปฏิกิริยาเคมี ในเซลล์ของสิ่งมีชีวิต ในเซลล์ของสิ่งมีชีวิต
ปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต มีทั้งการสังเคราะห์และการสลายสารชีวโมเลกุล มีทั้งการสังเคราะห์และการสลายสารชีวโมเลกุล ซึ่งเกี่ยวข้องกับการใช้พลังงานเคมีและการผลิตพลังงานเคมีของเซลล์ เมื่อเกิดปฏิกิริยาเคมี สารตั้งต้นเปลี่ยนแปลงเป็นสารผลิตภัณฑ์ และจะมีการเปลี่ยนแปลงพลังงานควบคู่ไปกับการเปลี่ยนแปลงพันธะเคมีด้วย ซึ่งเกี่ยวข้องกับการใช้พลังงานเคมีและการผลิตพลังงานเคมีของเซลล์ เมื่อเกิดปฏิกิริยาเคมี สารตั้งต้นเปลี่ยนแปลงเป็นสารผลิตภัณฑ์ และจะมีการเปลี่ยนแปลงพลังงานควบคู่ไปกับการเปลี่ยนแปลงพันธะเคมีด้วย
- เซลล์นำสารอาหารไปใช้กระบวนการต่างๆ
- กระบวนการต่างๆเหล่านี้จัดเป็น ปฏิกิริยาเคมีในเซลล์
ปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต แบ่งออกเป็น 2 ประเภท คือ
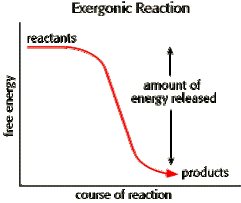
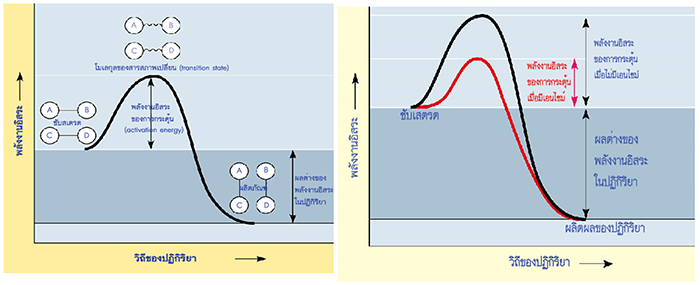
1. ปฏิกิริยาคายพลังงาน (Exergonic reaction) หมายถึง ปฏิกิริยาที่เกิดขึ้นแล้วจะปล่อยพลังงานออกมามากกว่าพลังงานกระตุ้นที่ใส่เข้าไป ทำให้พลังงานของสารตั้งต้นมีค่าสูงกว่าพลังงานของผลิตภัณฑ์
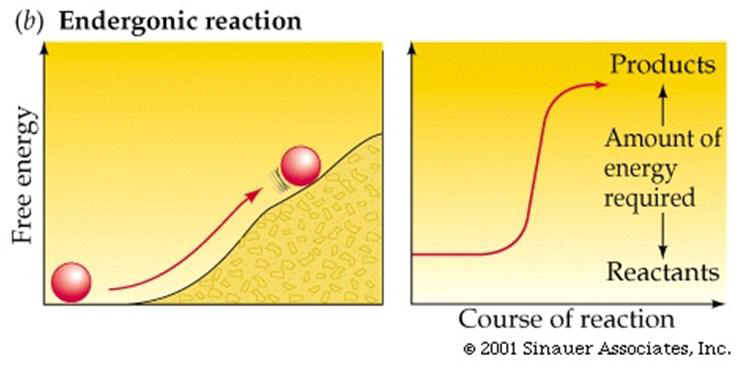
2. ปฏิกิริยาดูดพลังงาน (Endergonic reaction) หมายถึง ปฏิกิริยาที่เกิดขึ้นแล้วจะปล่อยพลังงานออกมาน้อยกว่าพลังงานกระตุ้นที่ใส่เข้าไป เช่น การแยกน้ำด้วยไฟฟ้า, การสังเคราะห์ด้วยแสง ทำให้พลังงานของผลิตภัณฑ์มีค่าสูงกว่าพลังงานของสารตั้งต้น ทำให้พลังงานของผลิตภัณฑ์มีค่าสูงกว่าพลังงานของสารตั้งต้น
สร้างคาย
- ปฏิกิริยาเคมีที่ "สร้าง" พันธะเคมี ขึ้นมาใหม่ ขึ้นมาใหม่
- เมื่อ "จบขั้นตอน" แล้วผลรวมของพลังงานในระบบ มีพลังงานที่เหลือจากปฏิกิริยาถูกปลดปล่อย ("คาย") ออกมาให้สิ่งแวดล้อม
สลายดูด
- ปฏิกิริยาเคมีที่มีการ "สลาย" พันธะเคมีไป
- เมื่อ "จบขั้นตอน" แล้วผลรวมของพลังงานในระบบ มีการ "ดูด" พลังงานความร้อนจากสิ่งแวดล้อมเข้าไป
องค์ประกอบของปฏิกิริยาเคมี
- สารตั้งต้น (Substrate)
- เอนไซม์ (Enzyme)
- ผลิตภัณฑ์ (Product)
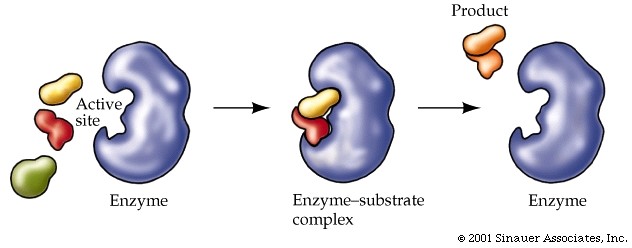

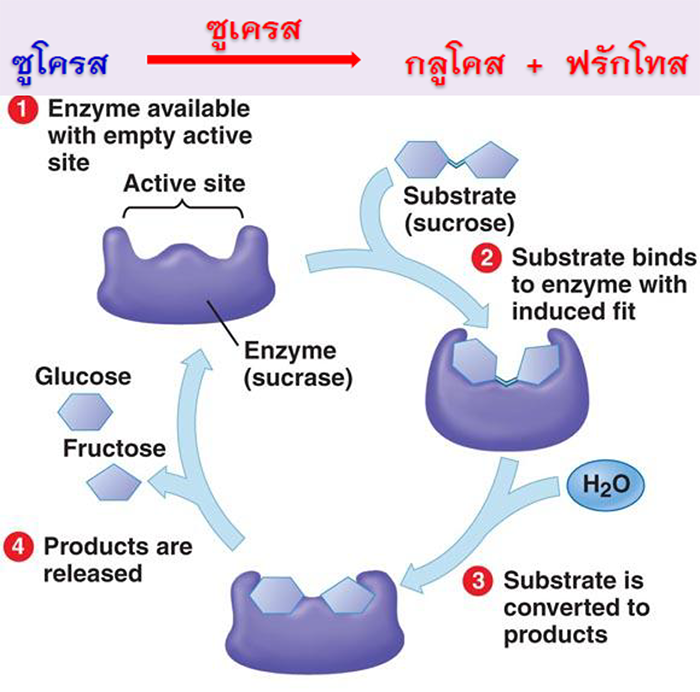
กลไกการทำงานของเอนไซม์ 
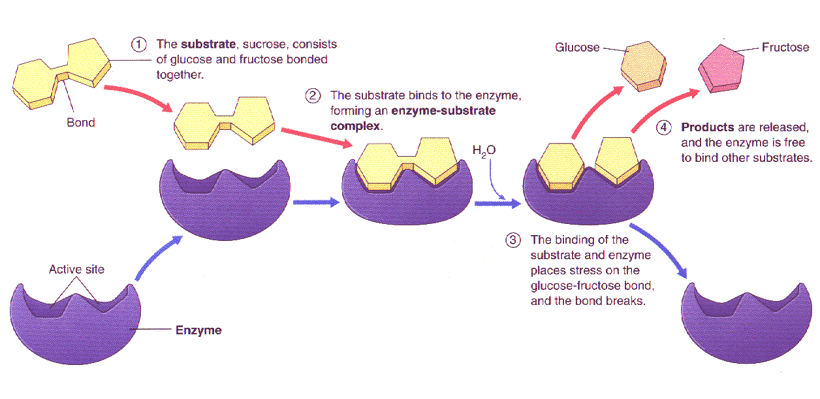
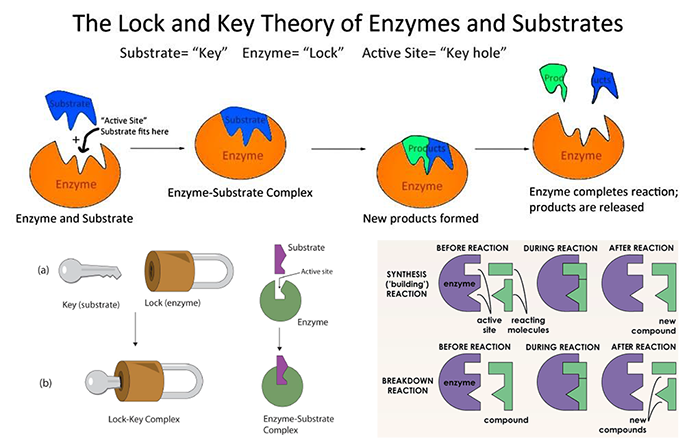
สมบัติของเอนไซม์
เป็นสารอินทรีย์  ประเภทโปรตีน ทำหน้าที่เป็นตัวเร่งปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต โดยการลดระดับพลังงานกระตุ้นลง ทำให้เกิดปฏิกิริยาง่ายขึ้น ประเภทโปรตีน ทำหน้าที่เป็นตัวเร่งปฏิกิริยาเคมีในเซลล์ของสิ่งมีชีวิต โดยการลดระดับพลังงานกระตุ้นลง ทำให้เกิดปฏิกิริยาง่ายขึ้น
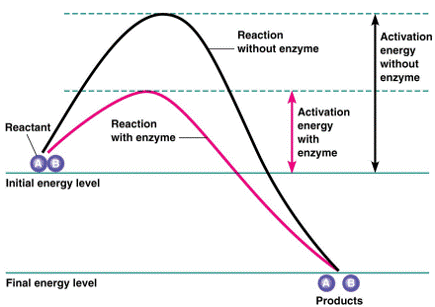
- ก่อนและหลังเกิดปฏิกิริยา เอนไซม์จะไม่เปลี่ยนแปลง
- เอนไซม์สามารถเร่งปฏิกิริยาเคมีได้อย่างมีประสิทธิภาพ แม้มีปริมาณเพียงเล็กน้อย
- เอนไซม์สามารถเร่งปฏิกิริยาได้โดยไม่ต้องใช้อุณหภูมิและความดันสูง
ปัจจัยที่มีผลต่อการทำงานของเอนไซม์
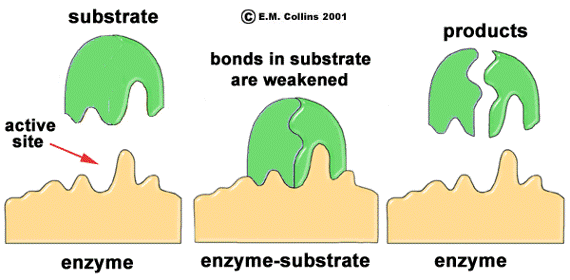
1. ชนิดของสารที่เอนไซม์ไปควบคุมปฏิกิริยา เอนไซม์แต่ละตัวทำงานเฉพาะสับสเตรตหนึ่งๆ เท่านั้น จะไม่ไปเกี่ยวข้องกับสับสเตรตอื่นๆ
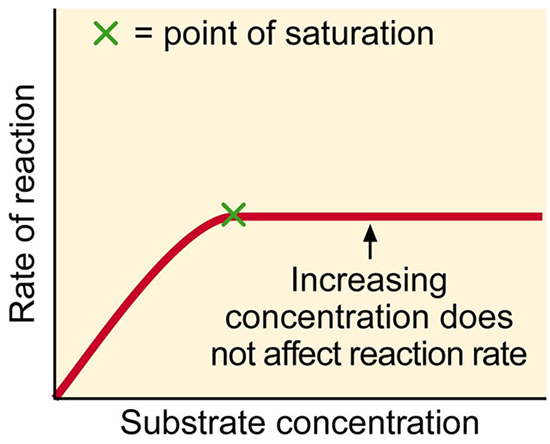
2. ความเข้มข้นของสับสเตรต
- เมื่อเอนไซม์คงที่ ถ้าเพิ่มความเข้มข้นของสับสเตรตจะทำให้อัตราเร่งปฏิกิริยาเพิ่มขึ้น จนถึงจุดๆ หนึ่งแล้วคงที่
- ถ้าความเข้มข้นของสับสเตรตเข้มข้นเกินไป จะทำให้เอนไซม์หยุดการทำงานได้
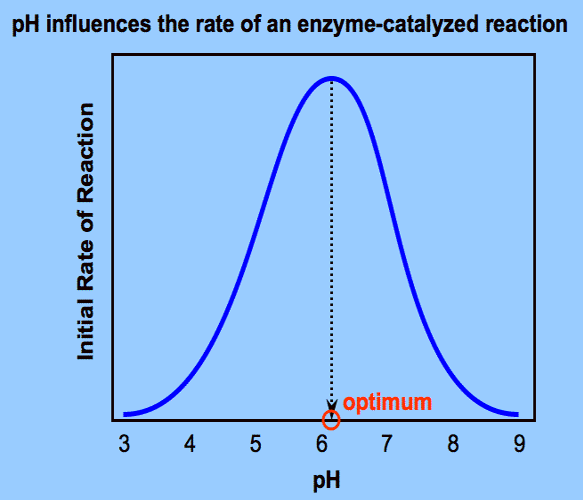
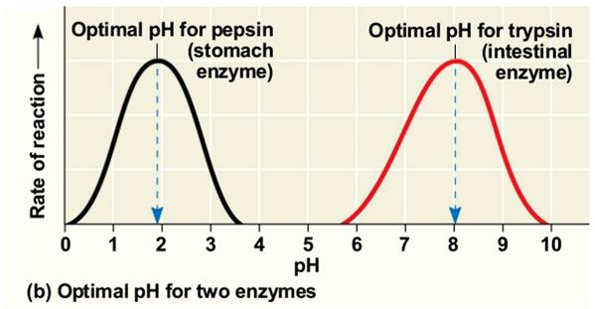
3. ความเป็นกรด-เบสของสารละลาย 
- เอนไซม์จะทำงานได้ดีที่สุดสำหรับค่า pH ค่าหนึ่ง
- ถ้าเปลี่ยน pH เล็กน้อยอาจจะทำให้อัตราการเกิดปฏิกิริยาของเอนไซม์ลดหรือเพิ่มขึ้นได้ เล็กน้อยอาจจะทำให้อัตราการเกิดปฏิกิริยาของเอนไซม์ลดหรือเพิ่มขึ้นได้
- ส่วนใหญ่อยู่ในช่วง pH 6 - 7.5
4. อุณหภูมิ
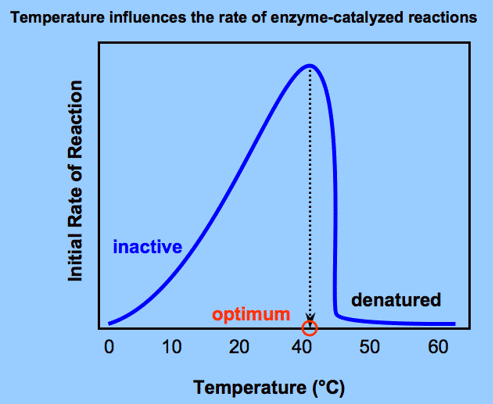
- การเพิ่มอุณหภูมิมีผลต่อปฏิกิริยาที่เร่งเอนไซม์ทั้งทางบวกและทางลบ
- การเพิ่มอุณหภูมิก็จะทำให้เอนไซม์ ซึ่งเป็นโปรตีน เปลี่ยนสภาพเดิมของมันได้ง่าย เปลี่ยนสภาพเดิมของมันได้ง่าย
- อุณหภูมิที่พอเหมาะอยู่ในช่วงอุณหภูมิ 25–40 oC
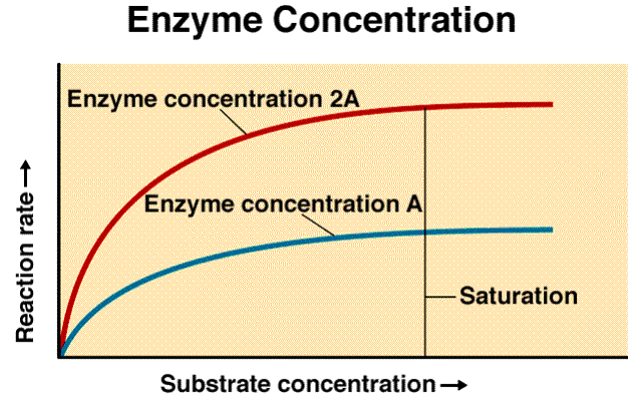
5. ความเข้มข้นของเอนไซม์ สับสเตรตประมาณหนึ่งนั้น ต้องใช้เอนไซม์ประมาณพอเหมาะ ถ้าเอนไซม์มากหรือน้อยไปก็จะทำงานได้ผลไม่เต็มที่
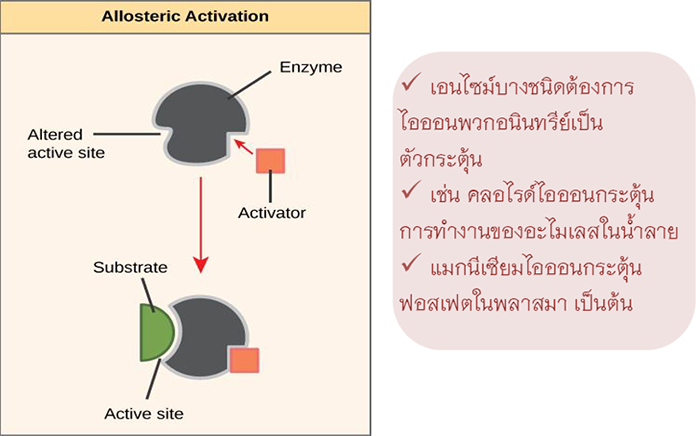
6. สารกระตุ้น (Activator)
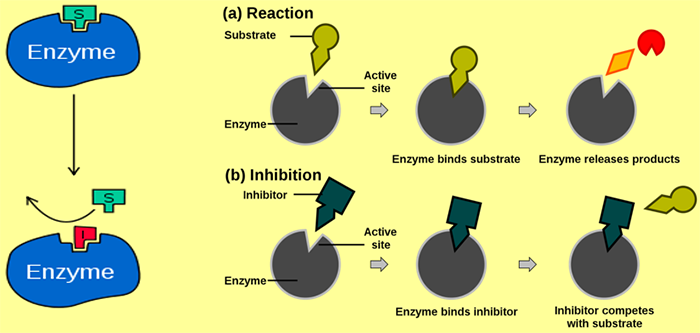
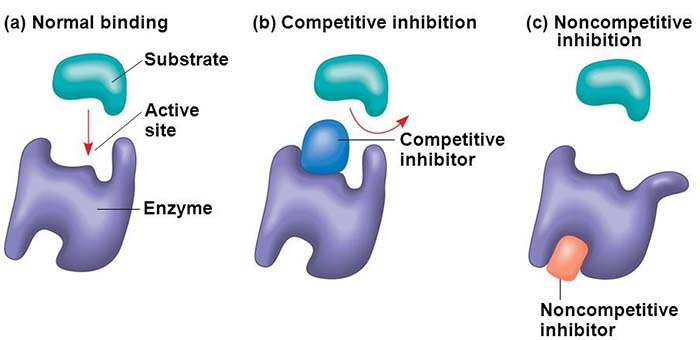
ตัวยับยั้งเอนไซม์
คือ สารที่ทำให้เอนไซม์เร่งปฏิกิริยาได้ลดลงหรือหยุดชะงัก








|

