

การระบุหน่วยของการวัดปริมาณต่าง ๆ ในชีวิตประจำวันความยาว มวล อุณหภูมิ อาจแตกต่างกันในแต่ละประเทศ เช่น การระบุน้ำหนักเป็นกิโลกรัม ปอนด์ หรือ การระบุส่วนสูงเป็น เซนติเมตร ฟุต ซึ่งทำให้ไม่สะดวกในการเปรียบเทียบหรือสื่อสารให้เข้าใจตรงกัน บางกรณี อาจนำไปสู่ความเข้าใจผิดที่ทำให้เกิดความเสียหายได้
ดังนั้น เพื่อให้การสื่อสารข้อมูลจากการวัดเป็น ที่เข้าใจตรงกัน จึงมีการตกลงร่วมกันให้มีหน่วยมาตรฐานสากลขึ้น

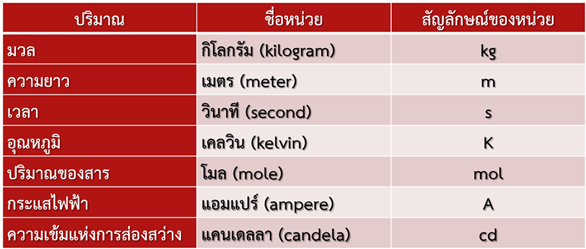
ในปี พ.ศ. 2503 ที่ประชุมนานาชาติว่าด้วยการ ชั่งและการวัด (The General conference on Weights and Measures) ได้ตกลงให้มีหน่วยวัดสากลขึ้น เรียกว่า ระบบหน่วยวัด ระหว่างประเทศ หรือ เรียกย่อ ๆ ว่า หน่วยเอสไอ (SI units) ซึ่งเป็นหน่วยที่ดัดแปลงจาก หน่วยในระบบเมทริกซ์โดยหน่วยเอสไอแบ่งเป็นหน่วยฐาน (SI base units) มี 7 หน่วย ซึ่งเป็นหน่วยที่ไม่ขึ้นต่อกัน และสามารถนำไปใช้ในการกำหนดหน่วยอื่น ๆ ได้และหน่วยเอสไออนุพันธ์ (Derived SI units) มี 7 หน่วย ซึ่งเป็นหน่วยที่ไม่ขึ้นต่อกัน และสามารถนำไปใช้ในการกำหนดหน่วยอื่น ๆ ได้และหน่วยเอสไออนุพันธ์ (Derived SI units)  ซึ่งเป็นหน่วยอื่น ๆ ที่มีความสัมพันธ์กันทางคณิตศาสตร์ของหน่วยเอสไอพื้นฐาน ซึ่งเป็นหน่วยอื่น ๆ ที่มีความสัมพันธ์กันทางคณิตศาสตร์ของหน่วยเอสไอพื้นฐาน
ตาราง ตัวอย่างหน่วยเอสไออนุพันธ์


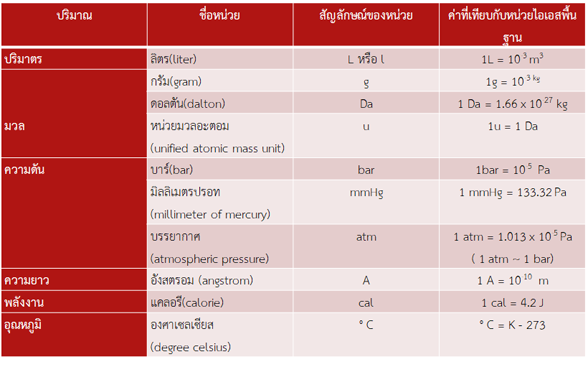
นอกจากหน่วยในระบบเอสไอแล้ว ในทางเคมียังมีหน่วยอื่นที่ได้รับ การยอมรับและมีการใช้กันอย่างแพร่หลาย ตัวอย่างดังตาราง

1. ลวดแมกนีเซียมหนา 0.1 มิลลิเมตร สามารถเขียนแสดงความหนาให้อยู่ในรูปสัญกรณ์ วิทยาศาสตร์ในหน่วยเอสไอได้เป็นเท่าใด
0.1 mm = 0.1 x 10-3 m = 1 x 10-4 m
2. ปริมาตรน้ำที่ได้จากปิเปตต์ 10.00 ลูกบาศก์เซนติเมตร สามารถเขียนแสดงปริมาตรให้อยู่ในรูปสัญกรณ์วิทยาศาสตร์ ในหน่วยเอสไอได้เป็นเท่าใด
1 cm3 = 1 cm x 1 cm x 1 cm
= 0.01 m x 0.01 m x 0.01 m
= 1 x 10-6 m3
ดังนั้น 10.00 cm3 = 10.00 x 10-6 m3
= 1.000 x 10-5 m3
ในทางวิทยาศาสตร์การคำนวณเกี่ยวกับปริมาณต่าง ๆ อาจจำเป็นต้องมีการเปลี่ยนหน่วยให้อยู่ในหน่วยที่เหมาะสม โดยไม่ทำให้ค่าของปริมาณเปลี่ยนแปลง เช่น ในทางเคมีนิยมระบุพลังงาน ในหน่วยแคลอรี ในขณะที่หน่วยเอสไอของพลังงานคือจูล ดังนั้น นักเคมีจึงจำเป็นต้องเปลี่ยนหน่วย พลังงานระหว่างแคลอรีและจูลเพื่อให้เหมาะสมกับการใช้งาน การเปลี่ยนหน่วยทำได้หลายวิธี ในที่นี้จะใช้วิธีการเทียบหน่วย ซึ่งต้องใช้แฟกเตอร์เปลี่ยนหน่วย

แฟกเตอร์เปลี่ยนหน่วย (conversion factors) เป็นอัตราส่วนระหว่างหน่วยที่แตกต่างกัน 2 หน่วย ที่มีปริมาณเท่ากัน
ตัวอย่างการหาแฟกเตอร์เปลี่ยนหน่วย เป็นดังนี้
จากความสัมพันธ์พลังงาน 1 cal = 4.2 J เมื่อใช้ 1 cal หารทั้งสองข้างจะได้เป็น
1 cal = 4.2 J
1 cal 1 cal
1 = 4.2 J
1 cal
หรือถ้าใช้ 4.2 J หารทั้งสองข้างจะได้เป็น
1 cal = 4.2 J
4.2 J 4.2 J
1 cal = 1
4.2 J
ดังนั้น แฟกเตอร์เปลี่ยนหน่วยเขียนได้เป็น 1 cal หรือ 4.2 J
ในทางคณิตศาสตร์เมื่อคูณปริมาณด้วย “1” จะทำให้ค่าของปริมาณเดิมไม่เปลี่ยนแปลง และแฟกเตอร์เปลี่ยนหน่วย และ ก็มีค่าเท่ากับ 1 ดังนั้นจึงสามารถนำแต่ละแฟกเตอร์ เปลี่ยนหน่วยไปใช้ในการเปลี่ยนหน่วยของปริมาณ ที่วัดจากหน่วยหนึ่งไปเป็นหน่วยอื่นโดยปริมาณ ไม่เปลี่ยนแปลง สำหรับตัวอย่างแฟกเตอร์เปลี่ยนหน่วยนี้ ใช้เปลี่ยนหน่วยจูลให้เป็นแคลอรีหรือแคลอรีให้เป็นจูล ตามลำดับ เช่น พลังงาน 20 cal สามารถเปลี่ยนเป็นหน่วยจูลได้ดังนี้ และ ก็มีค่าเท่ากับ 1 ดังนั้นจึงสามารถนำแต่ละแฟกเตอร์ เปลี่ยนหน่วยไปใช้ในการเปลี่ยนหน่วยของปริมาณ ที่วัดจากหน่วยหนึ่งไปเป็นหน่วยอื่นโดยปริมาณ ไม่เปลี่ยนแปลง สำหรับตัวอย่างแฟกเตอร์เปลี่ยนหน่วยนี้ ใช้เปลี่ยนหน่วยจูลให้เป็นแคลอรีหรือแคลอรีให้เป็นจูล ตามลำดับ เช่น พลังงาน 20 cal สามารถเปลี่ยนเป็นหน่วยจูลได้ดังนี้
พลังงาน = 20 cal x 4.2 J
1 cal = 84 J

วิธีการเทียบหน่วย (factor label method) ทำได้โดยการคูณปริมาณในหน่วยเริ่มต้นด้วย แฟกเตอร์เปลี่ยนหน่วยที่มีหน่วยที่ต้องการอยู่ด้านบน ตามสมการ
ปริมาณและหน่วยที่ต้องการ = ปริมาณและหน่วยเริ่มต้น x หน่วยที่ต้องการ
Ex.1 สารละลายกรดไฮโดรคลอริกมวล 20 กรัม ความหนาแน่น 1.18 กรัมต่อลูกบาศก์เซนติเมตร มีปริมาตรเท่าใด
วิธีทํา ปริมาตรของกรดไฮโดรคลอริก = 20 g solution x 1 cm3 solution
1.18 g solution = 16.95 cm3
คําตอบต้องมีเลขนัยสำคัญ 2 ตัว ดังนั้น สารละลายกรดไฮโดรคลอริกมีปริมาตร 17 ลูกบาศก์เซนติเมตร
แบบฝึกหัด
1. จงแสดงวิธีการเปลี่ยนหน่วยไปเป็นหน่วยใหม่ที่ต้องการในแต่ละข้อต่อไปนี้
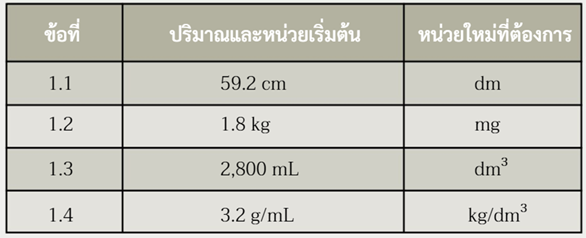

1.1 59.2 cm = 59.2 cm x 1 m x 10 dm
ดังนั้น 59.2 cm เท่ากับ 5.92 dm

1.2 1.8 kg = 1.8 kg x 1000 g x 1000 mg
ดังนั้น 1.8 kg เท่ากับ 1.8 x 106 mg

1.3 2,800 ml = 2,800 ml x 1 L x 1 dm3
ดังนั้น 2,800 mL อาจตอบได้เป็น 2.8 dm3 หรือ 2.80 dm3 หรือ 2.800 dm3
เนื่องจากเลขศูนย์อาจมีค่าเป็นศูนย์จริง ๆ จากการวัด หรือเป็นตัวเลขที่ใช้แสดงให้เห็นว่าค่าดังกล่าวอยู่ในหลักพัน

1.4 3.2 g/mL = 3.2 g x 1 kg x 1000mL x 1L
ดังนั้น 3.2 g/mL เท่ากับ 3.2 kg/ dm3
Ex.2 น้ำบริสุทธิ์ปริมาตร 50.0 ลูกบาศก์เซนติเมตร ที่อุณหภูมิ 20.5 องศาเซลเซียสมีมวลเท่าใด เมื่อความหนาแน่นของน้ำที่อุณหภูมิ 20.5 องศาเซลเซียส เท่ากับ 0.998099 กรัมต่อลูกบาศก์เซนติเมตร
มวลของน้ำ = 50 cm3 x 0.998099 g
1 cm3 = 49.90495 g
คำตอบต้องมีเลขนัยสำคัญ 3 ตัว ดังนั้น น้ำมีมวล 49.9กรัม
Ex.3 สารละลายกรดซัลฟิวริกเข้มข้นร้อยละ 24 โดยมวล มีความหนาแน่น 1.2 กรัมต่อลูกบาศก์เซนติเมตร ถ้าสารละลายกรดซัลฟิวริก 200 ลูกบาศก์เซนติเมตร จะมีกรดซัลฟิวริกกี่กรัม
ปริมาณกรดซัลฟิวริก = 24 g acid x 1.2 g solution x 200 cm3solution
คำตอบต้องมีเลขนัยสำคัญ 2 ตัว ดังนั้น มีกรดซัลฟิวริก 58 กรัม
Ex.4 ถ้าทองเหลือง 12 กรัม ต้องใช้ทองแดง 9.0 กรัม มีต้นทุนราคาของทองแดงกิโลกรัมละ 200 บาท หากต้องการทองเหลือง 300 กรัม ต้องซื้อทองแดงกี่บาท
ต้องซื้อทองแดง = 9.0 g Cu x 1 Kg Cu x 200 Baht x 300 g brass
คำตอบต้องมีเลขนัยสำคัญ 2 ตัว ดังนั้น ต้องซื้อทองแดง 45 บาท
แบบฝึกหัดท้ายบท
เติมเครื่องหมาย / หน้าข้อความที่ถูกต้อง และเครื่องหมาย x หน้าข้อความที่ไม่ถูกต้อง
……. 4.1 ข้างขวดน้ำดื่มยี่ห้อหนึ่งระบุว่าปริมาตรน้ำภายในขวดเท่ากับ 0.6 ลิตรหมายความว่าน้ำดื่มในขวดนั้นมีน้ำปริมาตร 600 มิลลิลิตร
……. 4.2 ใช้ปิเปตต์แบบปริมาตรขนาด 10 ลูกบาศก์เซนติเมตร ปิเปตต์สารละลาย A ถ่ายลงในบีกเกอร์ สารละลาย A ในบีกเกอร์มีปริมาตรเท่ากับ 10.00 มิลลิลิตร
……. 4.3 สารละลาย B ในขวดกำหนดปริมาตรขนาด 250 มิลลิลิตร หมายความว่าเมื่อเทสารละลาย B ออกมาใส่บีกเกอร์สามารถวัดปริมาตรได้เท่ากับ 250 มิลลิลิตร
……. 4.4 ในการไขสารละลายออกจากบิวเรตต์จะอ่านเลขทศนิยมของปริมาตรของ สารละลายได้ 2 ตําแหน่งเสมอ
……. 4.5 เมื่อตวงสารละลาย C โดยใช้กระบอกตวงให้มีปริมาตร 100.00 มิลลิลิตร แล้วเทใส่ในบีกเกอร์ขนาด 250 มิลลิลิตร จะสามารถอ่านปริมาตรของสารละลาย C ได้เท่ากับ 100.00 มิลลิลตร






|

