|
 การวิเคราะห์เชิงปริมาณ (quantitative analysis) ของสารละลาย ซึ่งเกี่ยวข้องความเข้มข้น (concentration) นักเคมีได้จำแนกความเข้มข้นแตกต่างกันไปตามหน่วยความเข้มข้น โดยทั่วไป มีดังนี้ การวิเคราะห์เชิงปริมาณ (quantitative analysis) ของสารละลาย ซึ่งเกี่ยวข้องความเข้มข้น (concentration) นักเคมีได้จำแนกความเข้มข้นแตกต่างกันไปตามหน่วยความเข้มข้น โดยทั่วไป มีดังนี้

 1. ร้อยละโดยมวล (percent mass by mass) เป็นอัตราส่วนร้อยละของมวลของตัวถูกละลายต่อมวลของสารละลาย มีสูตรดังนี้ 1. ร้อยละโดยมวล (percent mass by mass) เป็นอัตราส่วนร้อยละของมวลของตัวถูกละลายต่อมวลของสารละลาย มีสูตรดังนี้
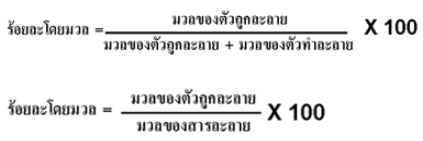
  เช่น x % โดยมวล คือสารละลาย 100 กรัม มีตัวถูกละลาย x กรัม เช่น x % โดยมวล คือสารละลาย 100 กรัม มีตัวถูกละลาย x กรัม
 2. ร้อยละโดยมวลต่อปริมาตร (percent mass by volume) เป็นอัตราส่วนร้อยละของมวลของตัวถูกละลายต่อปริมาตรของสารละลาย มีสูตรดังนี้ 2. ร้อยละโดยมวลต่อปริมาตร (percent mass by volume) เป็นอัตราส่วนร้อยละของมวลของตัวถูกละลายต่อปริมาตรของสารละลาย มีสูตรดังนี้

  เช่น x % โดยมวล/ปริมาตร คือสารละลาย 100 ลูกบาศก์เซนติเมตร มีตัวถูกละลาย x กรัม เช่น x % โดยมวล/ปริมาตร คือสารละลาย 100 ลูกบาศก์เซนติเมตร มีตัวถูกละลาย x กรัม
 3. ร้อยละโดยปริมาตรต่อปริมาตร (percent volume by volume) เป็นอัตราส่วนร้อยละของปริมาตรของตัวถูกละลายต่อปริมาตรของสารละลาย มีสูตรดังนี้ 3. ร้อยละโดยปริมาตรต่อปริมาตร (percent volume by volume) เป็นอัตราส่วนร้อยละของปริมาตรของตัวถูกละลายต่อปริมาตรของสารละลาย มีสูตรดังนี้

  เช่น x % โดยปริมาตร คือสารละลาย 100 ลูกบาศก์เซนติเมตร มีตัวถูกละลาย x ลูกบาศก์เซนติเมตร เช่น x % โดยปริมาตร คือสารละลาย 100 ลูกบาศก์เซนติเมตร มีตัวถูกละลาย x ลูกบาศก์เซนติเมตร

 เป็นอัตราส่วนของจำนวนโมลขององค์ประกอบแต่ละชนิดที่อยู่ในสารละลาย จะเขียนแทนด้วยสัญลักษณ์ X เพราะฉะนั้น ถ้าจะคำนวณหาเศษส่วนโมลของสาร A ในสารละลาย สามารถเขียนได้ดังนี้ เป็นอัตราส่วนของจำนวนโมลขององค์ประกอบแต่ละชนิดที่อยู่ในสารละลาย จะเขียนแทนด้วยสัญลักษณ์ X เพราะฉะนั้น ถ้าจะคำนวณหาเศษส่วนโมลของสาร A ในสารละลาย สามารถเขียนได้ดังนี้
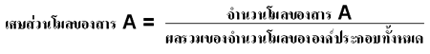

 โมลาริตี หรือ โมลาร์ เป็นหน่วยความเข้มข้น ที่เป็นอัตราส่วนของจำนวนโมลของตัวถูกละลายที่อยู่ในสารละลาย ปริมาตร 1 ลิตร (L) จะเขียนแทนด้วยสัญลักษณ์ M สามารถเขียนเป็นสูตรได้ดังนี้ โมลาริตี หรือ โมลาร์ เป็นหน่วยความเข้มข้น ที่เป็นอัตราส่วนของจำนวนโมลของตัวถูกละลายที่อยู่ในสารละลาย ปริมาตร 1 ลิตร (L) จะเขียนแทนด้วยสัญลักษณ์ M สามารถเขียนเป็นสูตรได้ดังนี้

 โมลาร์ มีหน่วยเป็น mol / L ปริมาตรของสารละลาย โดยทั่วไปจะบอกเป็นหน่วยมิลลิลิตร (mL) ดังนั้น ความสัมพันธ์หน่วยของปริมาตร ระหว่างมิลลิลิตรกับลิตร เป็นดังนี้ โมลาร์ มีหน่วยเป็น mol / L ปริมาตรของสารละลาย โดยทั่วไปจะบอกเป็นหน่วยมิลลิลิตร (mL) ดังนั้น ความสัมพันธ์หน่วยของปริมาตร ระหว่างมิลลิลิตรกับลิตร เป็นดังนี้
1 L มีค่าเท่ากับ 1000 mL

 โมแลลิตี หรือ โมแลล เป็นหน่วยความเข้มข้น ที่เป็นอัตราส่วนของจำนวนโมลของตัวถูกละลายต่อมวลของตัวทำละลายใน 1 กิโลกรัม (kg) จะเขียนแทนด้วยสัญลักษณ์ m สามารถเขียนเป็นสูตรได้ดังนี้ โมแลลิตี หรือ โมแลล เป็นหน่วยความเข้มข้น ที่เป็นอัตราส่วนของจำนวนโมลของตัวถูกละลายต่อมวลของตัวทำละลายใน 1 กิโลกรัม (kg) จะเขียนแทนด้วยสัญลักษณ์ m สามารถเขียนเป็นสูตรได้ดังนี้


 http://www.il.mahidol.ac.th/e-media/ap-chemistry2/liquid_solution/solution_concentrations.htm http://www.il.mahidol.ac.th/e-media/ap-chemistry2/liquid_solution/solution_concentrations.htm
|

