
ทฤษฎีออร์บิทัลโมเลกุล (molecular orbital theory ; MO theory )
ทฤษฎีออร์บิทัลโมเลกุล เป็นทฤษฎีที่ใช้อธิบายว่าทั้งโมเลกุลและอะตอม ต่างก็มีออร์บิทัลซึ่งเป็นที่ที่อิเล็กตรอนสามารถเข้ามาอยู่ได้ โดยแต่ละออร์บิทัลมีพลังงานต่างกันไป หลักการสำคัญของทฤษฎีออร์บิทัลโมเลกุลจะมองว่า อิเล็กตรอนในออร์บิทัลโมเลกุลไม่ได้อยู่ประจำที่ (delocalized electrons) แต่สามารถเคลื่อนที่ไปได้ทั่วทั้งโมเลกุล
ถ้าเป็นออร์บิทัลของ อะตอม เรียกว่า ออร์บิทัลอะตอม
ถ้าเป็นออร์บิทัลของ โมเลกุล เรียกว่า ออร์บิทัลโมเลกุล
ข้อดี ของทฤษฎีออร์บิทัลโมเลกุลสามารถทำนายการเกิดเป็นโมเลกุล สมบัติทางแม่เหล็ก และให้ความเข้าใจเกี่ยวกับสภาวะเร้าของโมเลกุล
การซ้อนเหลื่อมกันของออร์บิทัลอะตอม ทำให้เกิดออร์บิทัลโมเลกุลซึ่งแบ่งได้เป็น 2 แบบ คือ
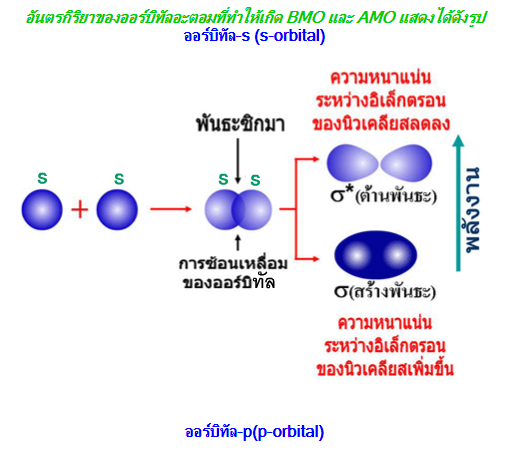
1. ออร์บิทัลโมเลกุลแบบสร้างพันธะ (bonding molecular orbital ; BMO) การเกิดออร์บิทัลโมเลกุลแบบนี้ จะทำให้อิเล็กตรอนมีพลังงานลดลง นั่นคือมีความเสถียรมากขึ้น
2. ออร์บิทัลโมเลกุลแบบต้านพันธะ (anti-bonding molecular orbital ; AMO) การเกิดออร์บิทัลโมเลกุลแบบนี้จะทำให้อะตอมที่ได้มีพลังงานเพิ่มขึ้น นั่นคือมีความเสถียรน้อยลง
ออร์บิทัล-p(p-orbital)
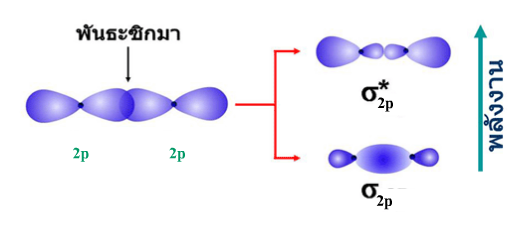
ก. ซ้อนเหลื่อมตามแนวปลาย
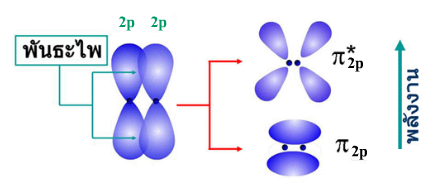
ข. ซ้อนเหลื่อมตามแนวข้าง
จากรูปแสดงการเกิดออร์บิทัลโมเลกุลิดจากการซ้อนเหลื่อมกันของออร์บิทัล-p
ก.ออร์บิทัล-p ทั้งสองเกิดการซ้อนเหลื่อมตามแนวปลายเกิดเป็นพันธะซิกมา ( σ-bond)
ข.ออร์บิทัล-p ทั้งสองเกิดการซ้อนเหลื่อมตามแนวข้างเกิดเป็นพันธะไพ (π-bond) "
จากรูปจะเห็นว่าออร์บิทัลโมเลกุลแบบสร้างพันธะจะมีพลังงานต่ำกว่าแบบต้านพันธะเสมอ ( * หมายถึงต้านพันธะ)
BMO และ AMO ที่ได้จากการรวมกันของออร์บิทัล -s จะแทนด้วยสัญลักษณ์ σs และ σ*sตามลำดับ
BMO และ AMO ที่ได้จากการรวมกันของออร์บิทัล -p จะแทนด้วยสัญลักษณ์ σz, σ* z, πx , π*x , πy , π*y ,πx,π*x ,πy , π*y
เมื่อ pz เกิดการซ้อนเหลื่อมตามแนวปลาย πx , πy เกิดการซ้อนเหลื่อมตามแนวข้าง
ขอบคุณเนื้อหาเพิ่มเติม
http://www.il.mahidol.ac.th/e-media/ap-chemistry1/chemical_bonding/covalent2.htm

|

