
เคมีเป็นพื้นฐานของสิ่งมีชีวิต (The Chemistry of Life)
ความเชื่อมโยงทางเคมีกับชีววิทยา 
A Chemical Connection to Biology
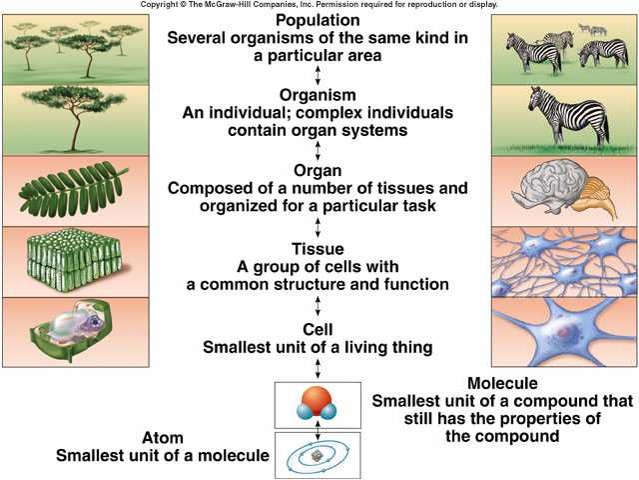
สสารเกิดจากธาตุเคมีที่อยู่ในรูปบริสุทธิ์ และจากการรวมกันของธาตุเหล่านั้นเป็นสารประกอบ
Matter consists of chemical elements in pure form and in combinations called compounds
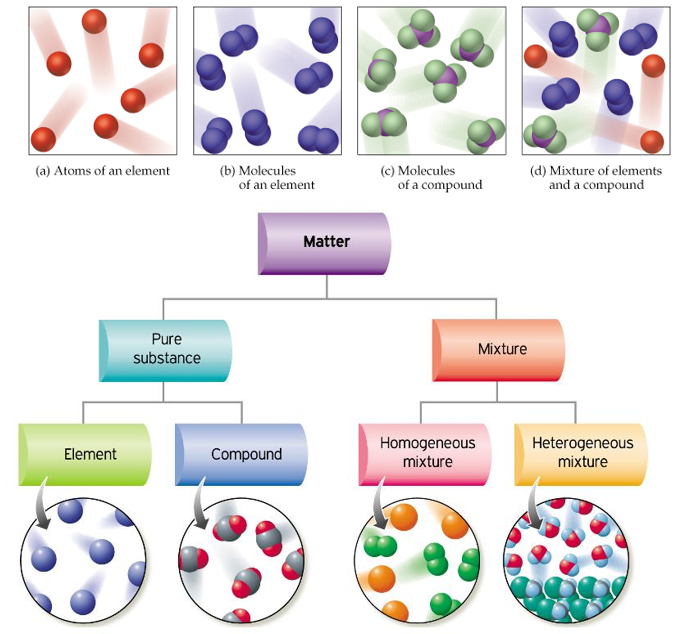
ธาตุ (Element) คือ สารบริสุทธิ์ที่ไม่สามารถแยกย่อยออกเป็นสารอื่นได้โดยวิธีปฏิกิริยาเคมีปฏิกิริยาเคมี  . .
An element is a substance that cannot be broken down to other substances by chemical reaction.

สารประกอบ (Compound) คือ สารที่เกิดจากธาตุที่แตกต่างกันตั้งแต่สองชนิดขึ้นไปรวมกันในอัตราส่วนที่แน่นอน
A compound is a substance consisting of two or more different elements combined in a fixed ratio.

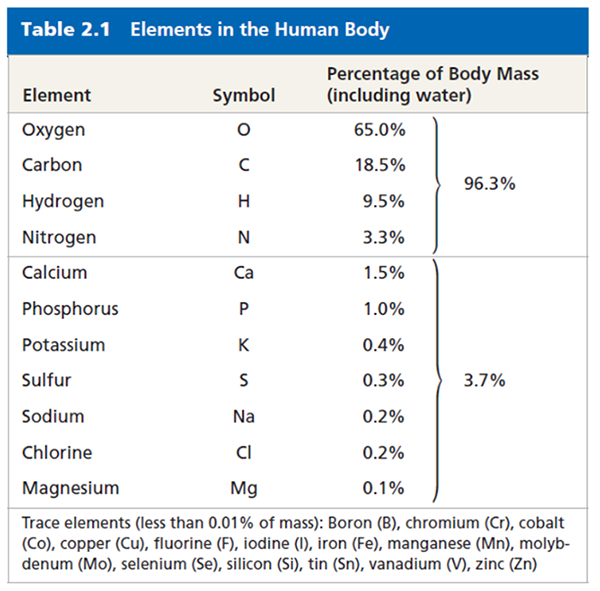
ปัจจุบัน นักเคมีสามารถระบุธาตุที่เกิดขึ้นตามธรรมชาติได้จำนวน 92 ธาตุ โดยแบ่งออกเป็นกลุ่มต่างๆ ดังนี้:
- ธาตุปริมาณมาก (Bulk element): ธาตุที่ร่างกายต้องการในปริมาณมากเพื่อการดำรงชีวิต เช่น คาร์บอน (C), ไฮโดรเจน (H), ออกซิเจน (O), และไนโตรเจน (N)
- ธาตุปริมาณน้อย (Trace element): ธาตุที่ร่างกายต้องการในปริมาณน้อย แต่มีความสำคัญต่อการทำงานของร่างกาย เช่น เหล็ก (Fe), สังกะสี (Zn), ทองแดง (Cu)
- ธาตุปริมาณน้อยมาก (Ultra trace element): ธาตุที่ร่างกายต้องการในปริมาณที่น้อยมาก แต่ยังจำเป็น เช่น ไอโอดีน (I), ซีลีเนียม (Se), โครเมียม (Cr)
Today, chemists recognize 92 elements occurring in nature.
- ธาตุปริมาณมาก (Bulk element)
- ธาตุปริมาณน้อย (Trace element)
- ธาตุปริมาณน้อยมาก (Ultra trace element)

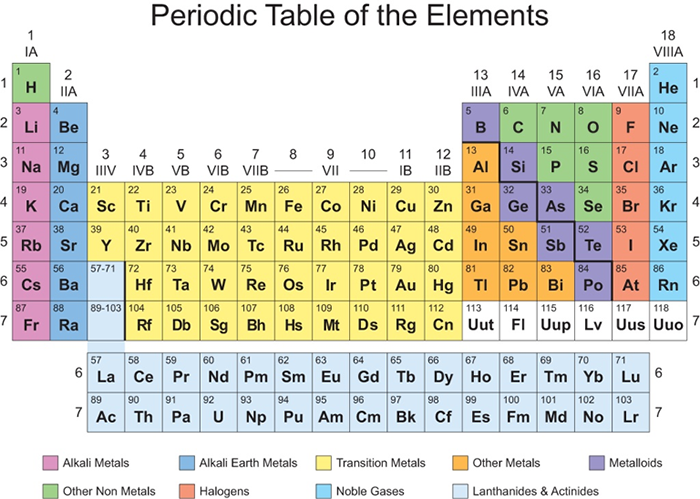
สมบัติของธาตุขึ้นอยู่กับโครงสร้างของอะตอม เลขอะตอม (Atomic Number) มวลอะตอม (Atomic Mass)
An element’s properties depend on the structure of its atoms 
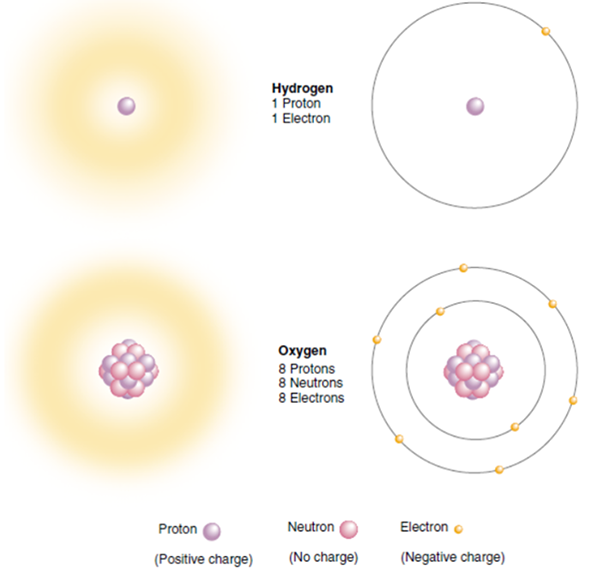
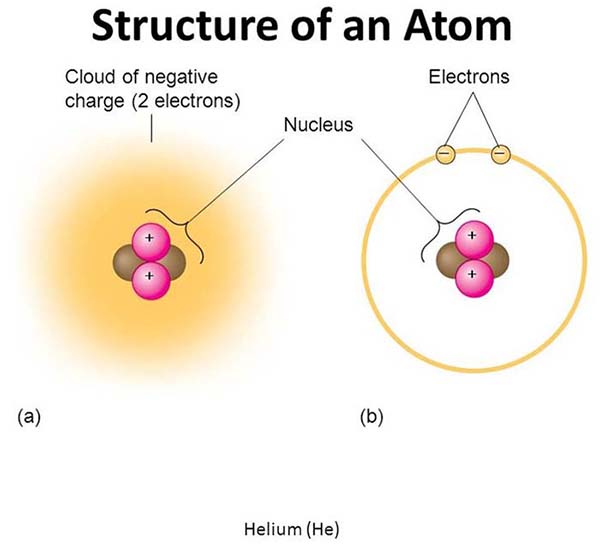

Atomic Number and Atomic Mass
เลขอะตอม (Atomic Number) คือ จำนวนโปรตอนที่อยู่ในนิวเคลียสของอะตอม ธาตุแต่ละชนิดจะมีเลขอะตอมเฉพาะตัว ซึ่งใช้กำหนดลำดับของธาตุในตารางธาตุ และบ่งบอกลักษณะเฉพาะของธาตุนั้น
มวลอะตอม (Atomic Mass) คือ มวลรวมของโปรตอนและนิวตรอนในนิวเคลียสของอะตอม โดยมีหน่วยเป็น amu (atomic mass unit) หรือเรียกอีกอย่างหนึ่งว่า มวลเชิงอะตอม ซึ่งใช้ในการเปรียบเทียบมวลของอะตอมต่างๆ

อะตอมของธาตุเดียวกันที่มีจำนวนโปรตอนเท่ากัน แต่จำนวนนิวตรอนต่างกัน
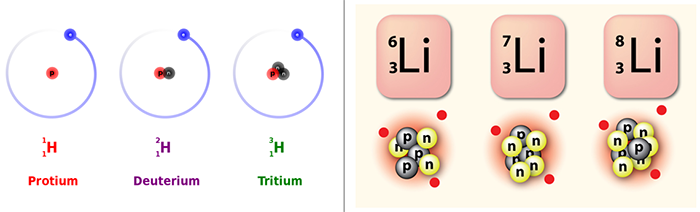
ระดับพลังงานของอิเล็กตรอน (The Energy Levels of Electrons)
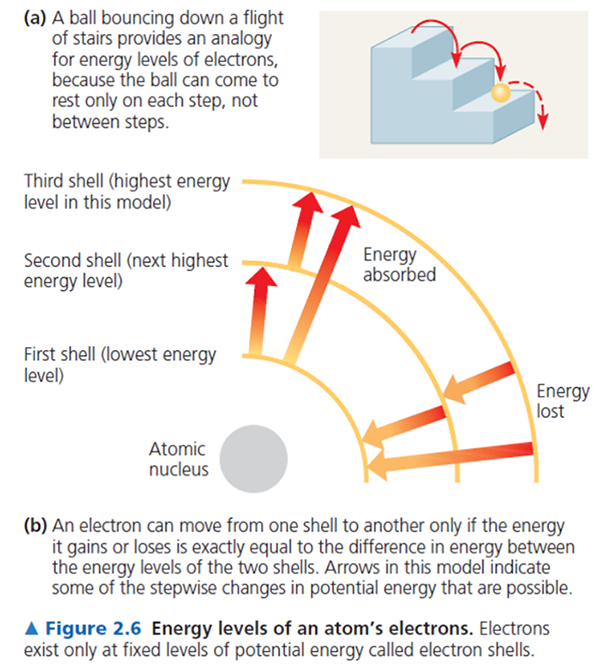
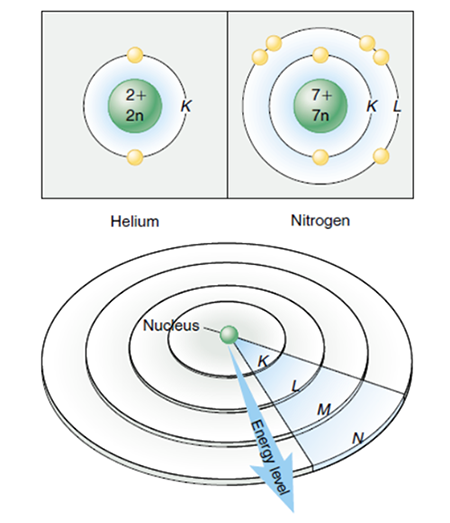
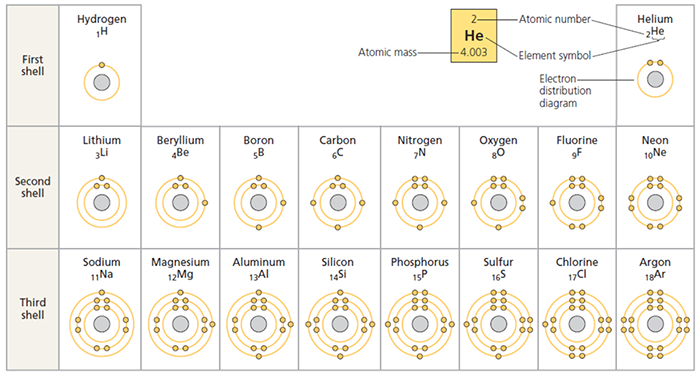
มีการจัดเรียงอิเล็กตรอนในระดับพลังงานต่าง ๆ ตามลำดับในตารางธาตุ (ภาพแสดงการแจกแจงอิเล็กตรอนของธาตุ 18 ชนิดแรก) (ภาพแสดงการแจกแจงอิเล็กตรอนของธาตุ 18 ชนิดแรก)
Electron distribution diagrams for the first 18 elements in theperiodic table
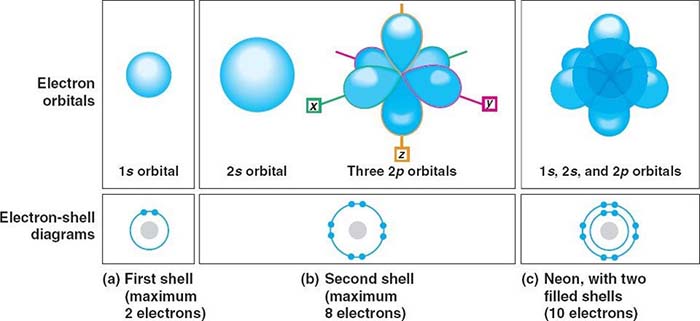
การสร้างและหน้าที่ของโมเลกุลขึ้นอยู่กับพันธะเคมีระหว่างอะตอม
The formation and function of molecules depend on chemical bonding between atoms.
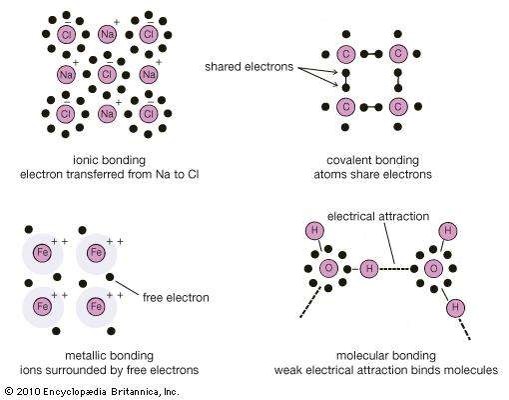
พันธะไอออนิก (Ionic Bond)
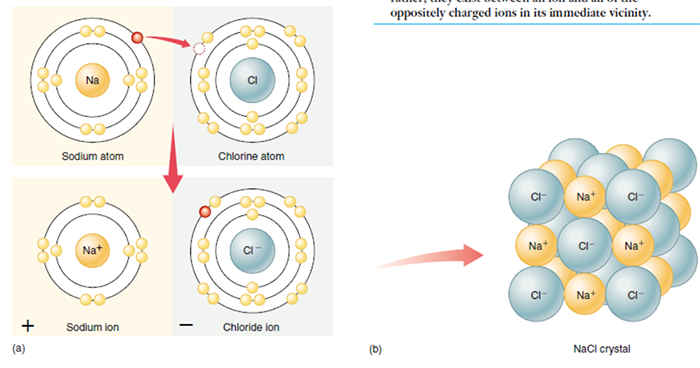
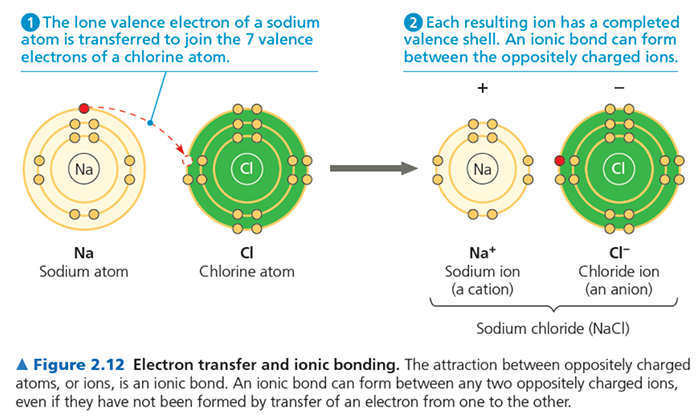

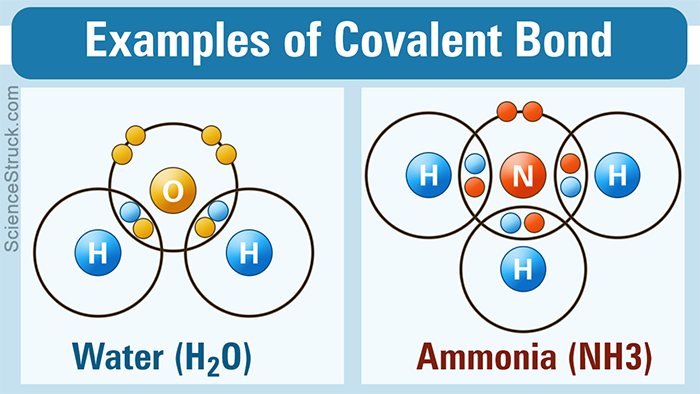
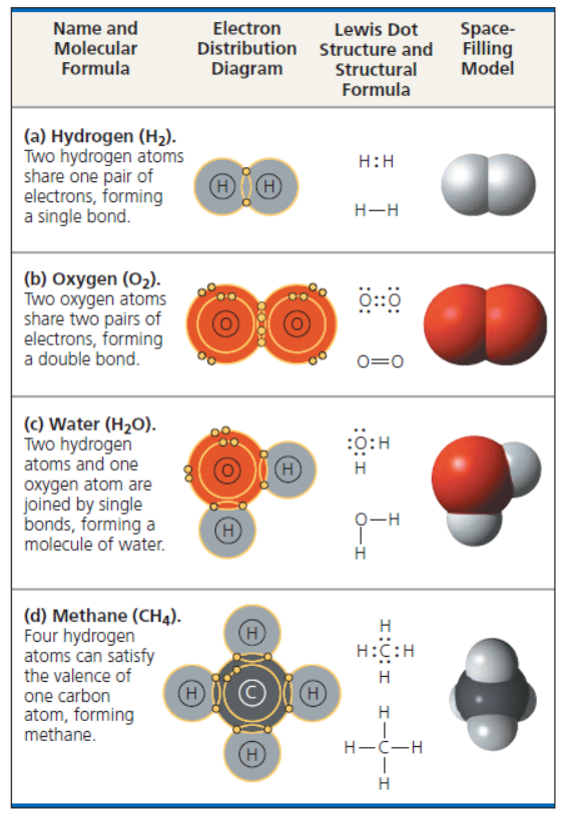
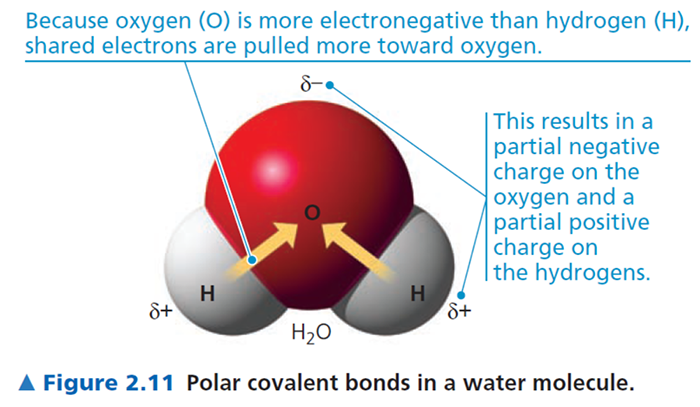
พันธะโคเวเลนต์เกิดจากการที่อะตอม แบ่งปันอิเล็กตรอนร่วมกัน เพื่อให้แต่ละอะตอมมีอิเล็กตรอนในระดับพลังงานนอกสุดครบตามที่ต้องการ (เสถียร)
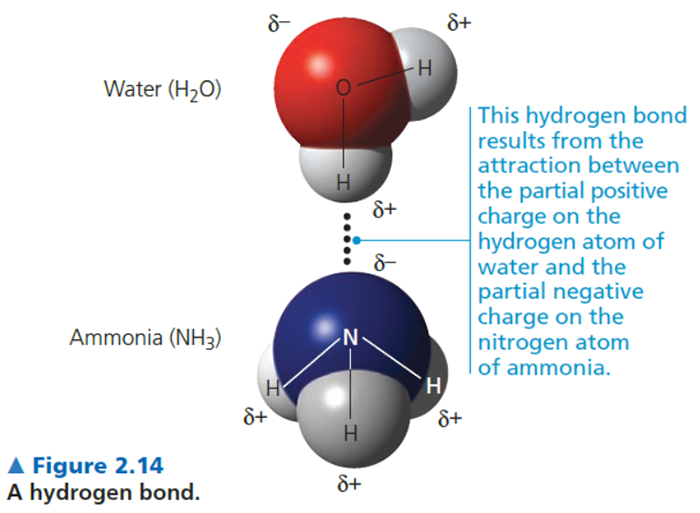


แรงแวนเดอร์วาลส์ (Van der Waals Interactions)
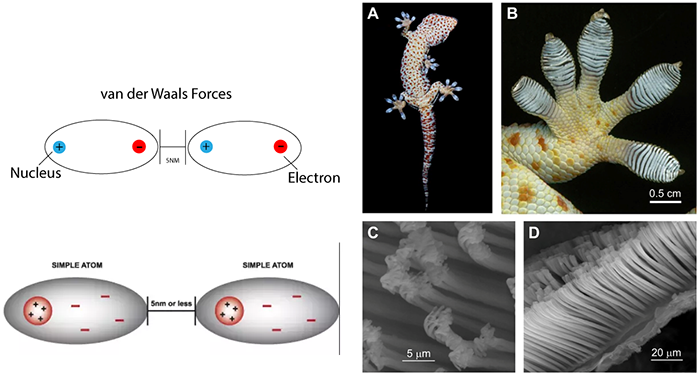
แรงแวนเดอร์วาลส์เป็นแรงยึดเหนี่ยวระหว่างโมเลกุลที่อ่อนมาก ซึ่งไม่ได้เกิดจากการถ่ายโอนหรือแบ่งปันอิเล็กตรอนโดยตรง แต่เกิดจากการเปลี่ยนแปลงชั่วคราวของการกระจายตัวของอิเล็กตรอนรอบๆ อะตอม ทำให้เกิดขั้วชั่วคราว (temporary dipole) ที่สามารถดึงดูดกันได้ระหว่างโมเลกุลใกล้เคียงกัน
สถานะของสสาร (State of matter)
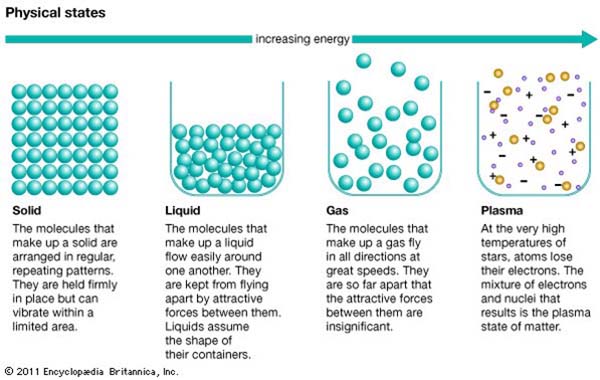
- ควบแน่นโบส-ไอน์สไตน์ (bose einstein condensate)
- ของแข็ง Solid
- ของเหลว (Liquid)
- แก๊ส (Gas)
- พลาสมา (Plasma)
- เส้นใย (Filament)
- ควบแน่นเฟอร์มิโอนิก (Fermionic condensate)







|

